· Ілля Добрий · ГДЗ · 7 хв. читати
§ 7 Властивості та принцип роботи ферментів
ПОМІРКУЙТЕ Й ОБГОВОРІТЬ СИТУАЦІЮ
Чому такі порошки не можна використовувати для прання речей із натуральних тканин (наприклад, шовку) чи за умов високої температури?
Натуральні тканини, такі як шовк або вовна, мають білкову природу, тому ферменти (протеази) у складі порошку розщеплюють волокна самої тканини, що призводить до її руйнування. Використання високих температур призводить до денатурації білків-ферментів, внаслідок чого вони втрачають свою об’ємну структуру та каталітичну активність.
Чи безпечно використовувати такі порошки для ручного прання?
Використання таких порошків для ручного прання без засобів захисту є небезпечним, оскільки ферменти можуть розщеплювати білки та жири, що входять до складу клітин шкіри людини, викликаючи подразнення, сухість або алергічні реакції.
ПОМІРКУЙТЕ Й ОБГОВОРІТЬ СИТУАЦІЮ
Чи існують якісь обмеження цього правила для ферментів? Якщо так, то чому?
Правило Вант-Гоффа має обмеження для ферментів, оскільки вони є білковими молекулами. При підвищенні температури понад оптимальні значення (зазвичай вище 40–50 °C) відбувається термічна денатурація ферменту, що спричиняє втрату його функцій та різке припинення хімічної реакції.
ПОДІЛІТЬСЯ СВОЇМИ ДУМКАМИ
Пригадайте й зазначте, які з-поміж зображених компонентів їжі розщеплюють амілаза, пепсин, ліпаза та трипсин.
Амілаза розщеплює вуглеводи (зокрема крохмаль), ліпаза забезпечує розщеплення жирів, а пепсин та трипсин розщеплюють білки.
ЗАВДАННЯ ДОСЛІДЖЕННЯ
1. Сформулюйте гіпотезу.
Активність ферменту каталази та швидкість реакції, яку він каталізує, залежать від температури та кислотності середовища, а також прямо пропорційно залежать від концентрації ферменту в тканинах до моменту насичення субстратом.
Чи існує залежність між активністю ферменту каталази та кислотністю або температурою середовища?
Залежність між активністю каталази та станом середовища існує, оскільки цей фермент є білком, структура якого руйнується за умов високих температур (денатурація) або різких змін кислотності, що призводить до втрати його каталітичних властивостей.
Чи існує залежність між швидкістю реакції, що каталізує фермент, та його кількістю чи концентрацією субстрату?
Швидкість реакції прямо залежить від кількості ферменту та концентрації субстрату, оскільки збільшення кількості активних центрів або молекул реагенту підвищує ймовірність їхньої взаємодії до моменту повного насичення ферменту.
2. На основі завдань та гіпотези сформулюйте мету дослідження.
Мета дослідження: експериментально визначити характер впливу температури, рівня pH середовища та концентрації ферменту на інтенсивність розщеплення гідроген пероксиду каталазою, що міститься в клітинах картоплі.
3. Об’єднайтеся в групи й виконайте експеримент.
Експериментальна частина виконана відповідно до пунктів А, Б, В та Г протоколу дослідження, наведеного в підручнику.
4. Зафіксуйте ваші результати. Позначте пробірки, де відбувається реакція (виділяються пухирці газу). Зазначте інтенсивність виділення пухирців: +++ — дуже інтенсивно, ++ — інтенсивно, + — наявні, – — майже відсутні.
| Номер пробірки | Умови експерименту | Інтенсивність виділення пухирців |
|---|---|---|
| 1 | Кімнатна температура (контроль) | +++ |
| 2 | Висока температура (окріп) | – |
| 3 | Низька температура (лід) | + |
| 4 | Кисле середовище (оцет) | + |
| 5 | Лужне середовище (амоніак) | ++ |
| 6 | Знижена концентрація ферменту | ++ |
| 7 | Відсутність ферменту (контроль) | – |
5. Яка пробірка слугувала контролем у цьому досліді? З якою метою використовували пробірку № 7, де був відсутній фермент?
Контролем у цьому досліді слугувала пробірка № 1, у якій ферментативна реакція відбувалася за оптимальних (кімнатних) умов. Пробірку № 7 використовували як негативний контроль для підтвердження того, що розкладання гідроген пероксиду відбувається саме завдяки ферменту каталазі, який міститься в картопляному пюре, а не спонтанно або під дією води.
6. Для цього дослідження визначте незалежні, залежні та контрольовані змінні.
Незалежними змінними у дослідженні є температура середовища, рівень кислотності (рН) та концентрація ферменту.
Залежною змінною є активність ферменту каталази, що вимірюється інтенсивністю виділення бульбашок кисню або об’ємом виділеного кисню за одиницю часу.
Контрольованими змінними є об’єм розчину гідроген пероксиду, маса картопляного пюре в пробірках (крім пробірки № 7) та час, протягом якого проводиться спостереження.
7. Побудуйте графік залежності швидкості ферментативної реакції від pH розчину. Який діапазон pH є оптимальним для роботи ферменту? Спрогнозуйте швидкість ферментативної реакції за умов, коли pH = 6,5.
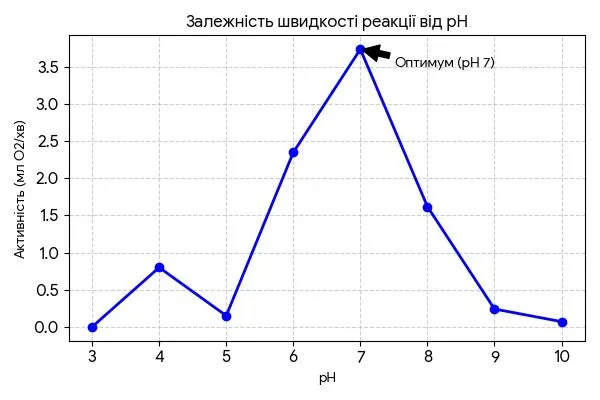
Оптимальним для роботи ферменту каталази є діапазон рН від 6 до 8, із піком активності за значення рН = 7. Прогнозована швидкість ферментативної реакції за умов, коли рН = 6,5, становить приблизно 3,05 мл /хв (середнє значення між показниками для рН 6 та рН 7).
8. З-поміж наведених графіків оберіть той, що відповідає залежності активності ферменту від температури.
Залежності активності ферменту від температури відповідає третій графік (дзвоноподібна крива з оптимумом). Активність ферменту зростає до досягнення певної температури (оптимуму), після чого різко падає через денатурацію білкової молекули ферменту.
9. Зробіть висновки.
Активність ферменту каталази безпосередньо залежить від умов довкілля: температури та рівня рН. Найвища активність спостерігається за нейтрального значення рН (близько 7) та кімнатної температури. Відхилення від оптимальних показників (кип’ятіння, сильне закислення або залужнення розчину) призводять до зниження швидкості реакції або повної зупинки через денатурацію білка-ферменту. Гідроген пероксид не розкладається самостійно без наявності каталізатора, що підтверджує біологічну роль ферментів у прискоренні хімічних процесів у живих організмах.
Чи підтвердилися висловлені вами гіпотези?
Висловлені гіпотези підтвердилися повністю: активність ферменту каталази безпосередньо залежить від температури середовища, рівня кислотності (pH) та концентрації субстрату.
Поясніть отримані результати активності ферменту за різних умов.
Найвища активність каталази спостерігається за кімнатної температури та нейтрального значення pH, що відповідає природним умовам функціонування клітин картоплі. У пробірці з окропом реакція відсутня, оскільки висока температура спричиняє денатурацію білка-ферменту та втрату його каталітичних властивостей. Зміна pH у кислий (додавання оцту) або лужний (додавання амоніаку) бік значно знижує активність ферменту через зміну конфігурації активного центру. Розведення витяжки водою призводить до зниження швидкості реакції внаслідок зменшення концентрації молекул ферменту в одиниці об’єму.
Зробіть загальний висновок про властивості ферментів.
Ферменти — це біологічні каталізатори білкової природи, які мають високу специфічність і працюють лише за певних оптимальних умов навколишнього середовища. Їхня активність є чутливою до змін температури та кислотності, а термічний вплив понад критичну межу призводить до незворотної втрати їхніх функцій через руйнування структури білка.
ПРОЄКТ «ВИКОРИСТАННЯ ФЕРМЕНТІВ У ПОБУТІ, МЕДИЦИНІ ТА СУЧАСНИХ ТЕХНОЛОГІЯХ»
1. Формулювання мети проекту; аргументування актуальності теми проекту; визначення джерел інформації; опрацювання зібраної інформації, її аналіз і узагальнення (на конкретних прикладах ферментів).
Метою проєкту є вивчення практичного застосування різних груп ферментів у життєдіяльності людини та промисловості. Актуальність теми зумовлена необхідністю впровадження енергоефективних та екологічно безпечних біотехнологій, що замінюють агресивну хімічну дію. Джерелами інформації є науково-популярні видання, дані біотехнологічних підприємств та інструкції до фармакологічних засобів. Аналіз зібраних даних показує, що протеази та ліпази є основними компонентами сучасних засобів для прання, оскільки вони ефективно видаляють органічні плями за низьких температур. У харчовій промисловості фермент лактаза використовується для виготовлення безлактозної продукції, що забезпечує потреби людей із харчовою непереносимістю.
2. Створення самостійного інформаційного продукту (оригінального тексту) та формулювання висновків.
Ферменти стали невід’ємною частиною сучасної цивілізації. У медицині препарати на основі панкреатину допомагають компенсувати недостатність травних засобів, а фермент стрептокіназа використовується для розчинення тромбів у судинах. Текстильна промисловість використовує целюлази для обробки тканин, що надає їм м’якості та запобігає утворенню ковтунців. Висновки: завдяки своїй високій специфічності та здатності працювати в м’яких умовах, ферменти дозволяють створювати ефективні ліки та екологічні виробничі процеси. Використання ензимів значно підвищує якість життя людини та сприяє збереженню довкілля через зменшення використання агресивних хімікатів.
3. Оформлення результатів проекту (презентація, відеоролик, подкаст, буклет тощо).
Результати проекту оформлені у вигляді мультимедійної презентації, що містить графічні моделі, аналіз фармацевтичних препаратів та теоретичне обґрунтування властивостей ферментів.
ЗАПИТАННЯ І ЗАВДАННЯ
1. Розгляньте енергетичні ефекти хімічної реакції без каталізатора (синій колір графіка) та за наявності ферментів (бузковий колір графіка). У чому принципова відмінність каталізованої ферментом реакції від некаталізованої? Грунтуючись на зміні енергії реагентів та продуктів, зазначте, чи є ця реакція ендотермічною, чи вона — екзотермічна.
Принципова відмінність полягає у значному зниженні енергії активації: фермент дозволяє реакції відбуватися через проміжні стадії, які потребують менших енергетичних витрат для подолання бар’єру. Спираючись на графік, ця реакція є екзотермічною, оскільки рівень енергії продуктів нижчий за рівень енергії реагентів, що свідчить про виділення енергії в навколишнє середовище.
2. Використовуючи різноманітні матеріали (папір, картон, нитки, намистини, пластилін тощо), виготовте модель ферментативної реакції або зробіть віртуальну модель засобами графічного комп’ютерного дизайну. Презентуйте результати своєї роботи. Чи вдалося вам створити модель, яка просто пояснює механізм роботи ферменту?
Результати роботи представлені у вигляді віртуальної моделі, створеної засобами комп’ютерного дизайну, де активний центр ферменту має специфічну форму, що відповідає формі молекули субстрату. Створена модель успішно та просто пояснює механізм роботи ферменту за принципом «ключа та замка», демонструючи утворення фермент-субстратного комплексу та подальше перетворення субстрату на продукти.
3. Реклама часто пропонує нам після переїдання та важкості в животі вживати таблетки, що полегшують наш стан. Знайдіть подібні препарати та проаналізуйте їхню інструкцію. Які діючі речовини містять такі препарати? Який механізм їхньої дії? Чи безпечно їх уживати без призначення лікаря? Які існують протипоказання / побічні ефекти застосування цих препаратів?
До таких препаратів належать «Мезим», «Панкреатин», «Креон» та «Фестал», діючою речовиною яких є панкреатин — суміш ферментів підшлункової залози (амілази, ліпази та протеаз). Механізм їхньої дії полягає у компенсації дефіциту власних ферментів, що сприяє швидкому та повному розщепленню білків, жирів і вуглеводів у дванадцятипалій кишці. Систематичне вживання цих препаратів без призначення лікаря є небезпечним, оскільки може призвести до зниження природної активності підшлункової залози. Основними протипоказаннями є гострий панкреатит або загострення хронічного панкреатиту, а побічні ефекти включають алергічні реакції, нудоту, діарею або запор.
Оцініть матеріал
Натисніть на зірку для оцінки:
Коментарі
Залишити відповідь:
Ваша e-mail адреса не оприлюднюватиметься