· Ілля Добрий · ГДЗ · 3 хв. читати
Навчальне дослідження № 10
Навчальне дослідження № 10 «Залежність між масою реактанту та масою продуктів реакції»
Обладнання: ваги, мірний посуд (циліндр), хімічні склянки, скляна паличка, шпатель, лійка, фільтрувальний папір.
Речовини: розчин кальцій хлориду (, 5%), розчин натрій карбонату (соди, , 5%), дистильована вода.
1. Сформулюйте гіпотезу щодо чинників, які можуть уплинути на точність результатів дослідження.
Точність результатів залежить від повноти проходження реакції, точності зважування та можливих втрат речовини під час фільтрування (частина осаду може залишитися на стінках склянки або пройти крізь фільтр).
2. Використовуємо розчин кальцій хлориду з характеристиками:
3. Під час експерименту відбувається реакція відповідно хімічного рівняння:
4. Обчисліть об’єм розчину соди, необхідний для реакції з кальцій хлоридом.
Відомо:
Обчислити:
Розв’язання:
:
За рівнянням .
Відповідь: Потрібно 9,6 мл розчину соди.
5) Результати експерименту:
(6) Обчислення за рівнянням реакції маси кальцій карбонату (теоретичної):
Відомо:
- (з пункту 4)
Знайти:
Розв’язання:
Відповідь: Теоретично має утворитися 0,45 г.
7 Оцініть відносний вихід продукту реакції — частку кальцій карбонату, яку ви одержали від того, що мали одержати:
Ми отримали 0,40 г осаду, а теоретично мало бути 0,45 г.
Вихід продукту: .
Різниця виникла через втрати під час фільтрування та промивання осаду, що підтверджує нашу гіпотезу.
8. За даними вашого експерименту та даними інших груп складіть графік залежності маси продукту реакції від об’єму початкового розчину кальцій хлориду.
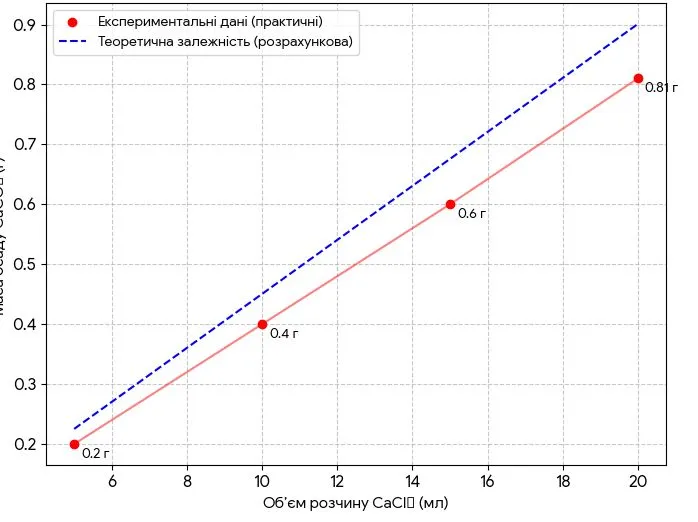
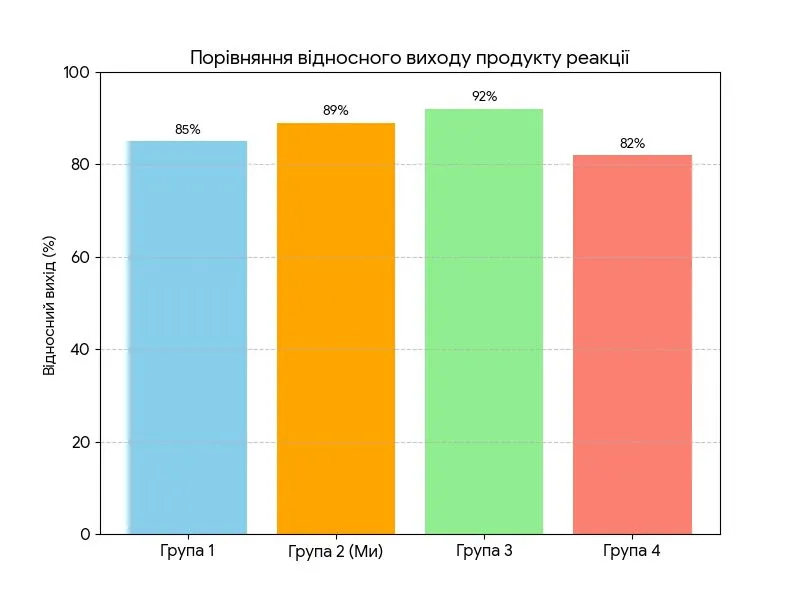
9. Порівняйте відносний вихід продукту реакції, отриманий вами й іншими групами ваших однокласників / однокласниць, склавши стовпчикову діаграму.
Підбиваємо підсумки
1. Чи збігається обчислена маса осаду з одержаною? Поясніть цей факт.
Ні, одержана (практична) маса осаду виявилася меншою за обчислену (теоретичну). Це сталося через неминучі виробничі втрати: частина речовини залишилася на стінках хімічної склянки, на скляній паличці або на самому фільтрі.
2. У якої групи найбільше відрізняються маса одержаного осаду та обчислене значення маси осаду (найменше значення відносного виходу продукту реакції)? Які чинники можуть упливати на цю різницю?
Найбільша різниця (і найменший вихід — 82%) спостерігається у 4-ї групи (за даними діаграми). На це могли вплинути: неточне вимірювання об’єму розчинів мензуркою, проливання частини розчину або неакуратне перенесення осаду на фільтр.
3. Чи вдалося підтвердити / спростувати гіпотезу, сформульовану вами до дослідження?
Так, гіпотезу вдалося підтвердити. Маса продукту реакції () прямо пропорційно залежить від об’єму (а отже, і маси) початкового розчину .
Оцініть матеріал
Натисніть на зірку для оцінки:
Коментарі
Залишити відповідь:
Ваша e-mail адреса не оприлюднюватиметься